Métodos de reemplazo para pruebas cosméticas
La cosmética sin crueldad avanza gracias a métodos alternativos como piel humana reconstruida y modelos computacionales. Son más éticos, precisos y ya están revolucionando la industria en todo el mundo.
El avance de la cosmética responsable ha estado íntimamente ligado al desarrollo de métodos científicos que permitan evaluar la seguridad de productos sin causar daño a animales. En respuesta a décadas de prácticas invasivas como el test de Draize, la ciencia moderna ha dado paso a un abanico de métodos alternativos, denominados NAMs; herramientas validadas que sustituyen el uso de animales en ensayos toxicológicos, especialmente en el sector cosmético.
En este nuevo paradigma, el objetivo no es solo evitar la crueldad, sino también mejorar la relevancia científica de los datos obtenidos. Estudios han demostrado que muchos de estos métodos alternativos tienen una mayor capacidad predictiva sobre la fisiología humana que los modelos animales, reduciendo la tasa de falsos positivos y negativos en pruebas de irritación, corrosión, fototoxicidad o sensibilización cutánea.
En esta búsqueda por erradicar el uso de animales en las pruebas cosméticas, han surgido laboratorios y plataformas científicas en todo el mundo que han adoptado enfoques innovadores y altamente eficientes para realizar evaluaciones de seguridad sin necesidad de experimentación animal. Este fenómeno se ha consolidado especialmente en Europa y América del Norte, pero también está ganando terreno en América Latina y otras regiones. Laboratorios como Episkin y SkinEthic se han destacado en la creación de modelos de piel humana reconstruida, lo que ha permitido la sustitución de animales en pruebas de irritación dérmica y ocular. Episkin es reconocido mundialmente por ser líder en ingeniería de tejidos humanos para pruebas in vitro, ofreciendo modelos de epidermis humana que replican con alta fidelidad la respuesta de la piel humana ante sustancias cosméticas.
Uno de los avances más importantes en el uso de piel humana reconstruida, son los modelos SkinEthic™ y EpiDerm™, capaces de imitar con gran fidelidad las capas de la epidermis, y que han sido aprobados por organismos regulatorios como la OECD, para testear cosméticos y sustancias químicas con alto grado de precisión, replicando la respuesta humana sin dañar a ningún animal. Los modelos de irritación ocular también han ganado un espacio importante en el desarrollo de NAMs, como SkinEthic™ HCE o EpiOcular™ que han reemplazado con éxito el test de Draize, obteniendo resultados más fiables sin utilizar conejos u otros animales.
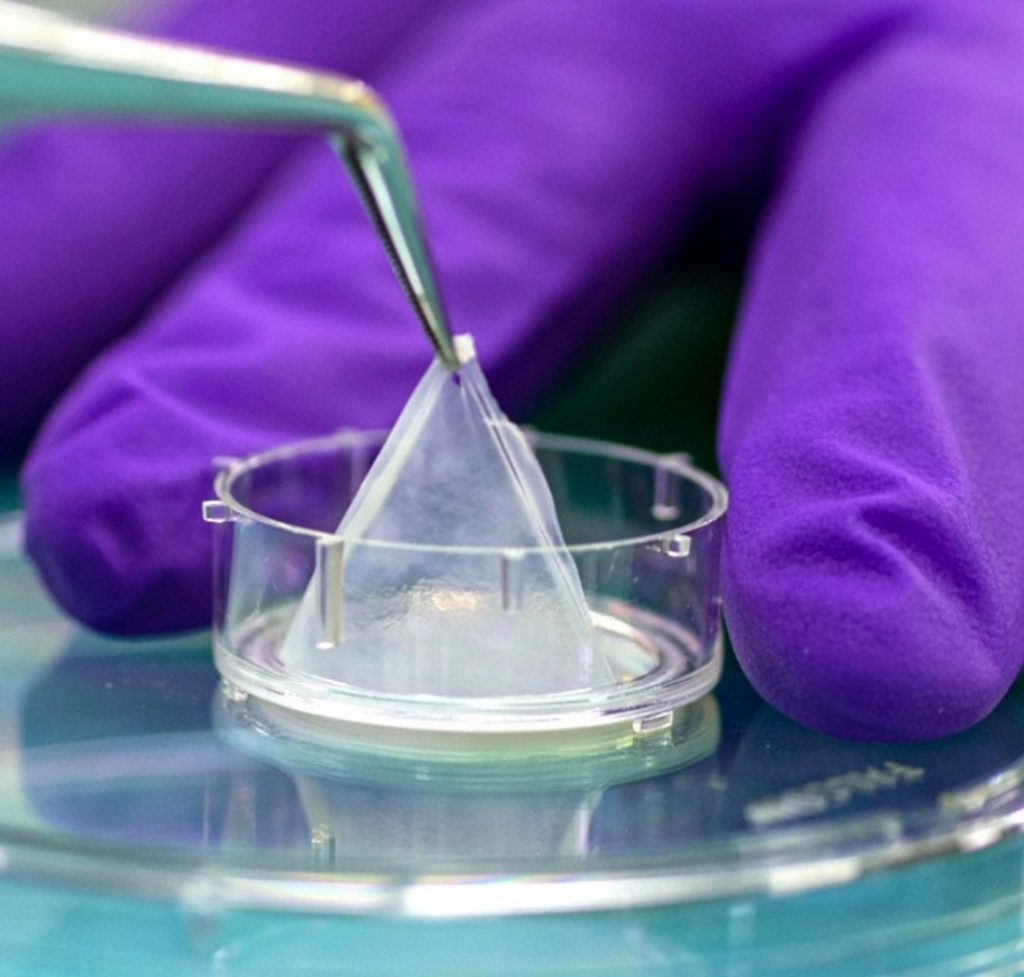
SkinEthic HCE validado por la OECD para el método de prueba TG492B.
Laboratorios alternativos
A pesar de que América Latina ha comenzado a seguir el ritmo de Europa y América del Norte, aún enfrenta retos regulatorios y económicos para la adopción generalizada de métodos alternativos. Sin embargo, países como Brasil han comenzado a aplicar la legislación internacional que promueve el reemplazo de los ensayos animales. Asimismo, existen laboratorios en la región que han dado un paso adelante al aplicar modelos de piel humana reconstruida, como LIALT en México, que utiliza modelos similares a los de SkinEthic para la prueba de irritación cutánea y fototoxicidad, el Laboratorio de Métodos Alternativos (LMA) en Argentina, que ofrece ensayos alternativos a sensibilización e irritación dérmica y ocular, mientras que Novum Science de Colombia y Functional Life en Chile ofrecen servicios de pruebas utilizando técnicas de cultivo celular y modelos 3D.
A nivel internacional, países como India, Noruega y regiones como la Unión Europea han legislado prohibiciones totales o parciales al testeo cosmético en animales, promoviendo la transición hacia NAMs. Organismos como la FDA (EE. UU.) y la EMA (Agencia Europea de Medicamentos) también han reconocido la eficacia de estos métodos para estudios preclínicos, consolidando su aceptación en la comunidad científica. Iniciativas como ICCVAM, EURL-ECVAM y la OECD continúan validando y ampliando el catálogo de NAMs aplicables a cosméticos, medicamentos y productos químicos.
Además de los métodos in vitro, el uso de modelos computacionales y la predicción por relaciones cuantitativas estructura-actividad (QSAR) se está expandiendo como una solución complementaria. Estas tecnologías analizan miles de compuestos en base a su estructura química, prediciendo toxicidad sin necesidad de ensayos físicos en animales, lo que permite ahorrar recursos, tiempo y evitar sufrimiento.
La ciencia ya demostró que es posible proteger la salud humana sin dañar a otras especies. Hoy, la pregunta no es si podemos reemplazar el testeo en animales, sino por qué seguimos justificándolo cuando existen opciones superiores.

Conejos y cuyes en bioterio. Understanding Animal Research.
Bibliografía.
- Episkin, (2024). World leader in tissue engineering for in vitro human skin and epithelial models. Retrieved from https://www.episkin.com/
- Capowski, E. E., Samimi, K., Mayerl, S. J., Phillips, M. J., Pinilla, I., Howden, S. E., Saha, J., Jansen, A. D., Edwards, K. L., Jager, L. D., Barlow, K., Valiauga, R., Erlichman, Z., Hagstrom, A., Sinha, D., Sluch, V. M., Chamling, X., Zack, D. J., Skala, M. C., & Gamm, D. M. (2019). Reproducibility and staging of 3D human retinal organoids across multiple pluripotent stem cell lines. Development (Cambridge, England), 146(1), dev171686. https://doi.org/10.1242/dev.171686
- Gamm, D. (2022, February 8). UW study finds photoreceptor cells from retinal organoids can replicate key functions of vision. Waisman Center. https://www.waisman.wisc.edu/2022/02/08/uw-study-finds-photoreceptor-cells-from-retinal-organoids-can-replicate-key-functions-of-vision/
- S. Food and Drug Administration. (2024, October 1). New Approach Methods (NAMs). https://www.fda.gov/food/toxicology-research/new-approach-methods-nams
- Kandárová, H., Hayden, P., Klausner, M., Kubilus, J., & Sheasgreen, J. (2009). An in vitro skin irritation test (SIT) using the EpiDerm reconstructed human epidermal (RHE) model. Journal of visualized experiments : JoVE, (29), 1366. https://doi.org/10.3791/1366
- Bajot F. (2010) The Use of Qsar and Computational Methods in Drug Design. In: Puzyn T., Leszczynski J., Cronin M. (eds) Recent Advances in QSAR Studies. Challenges and Advances in Computational Chemistry and Physics, vol 8. Springer, Dordrecht. https://doi.org/10.1007/978-1-4020-9783-6_9.
- Bhatia, S. N., & Ingber, D. E. (2014). Microfluidic organs-on-chips. Nature Biotechnology, 32(8), 760–772. https://doi.org/10.1038/nbt.2989
- User’s Manual. (2013). Three-dimensional cultured human cornea epithelial model. Retrieved, from: https://www.jpte.co.jp/en/business/LabCyte/cornea-model/documents/LabCyte_CORNEA-MODEL_Instruction_Manual_Mar2017.pdf
Comparte:
Copiar URL Más posts de raquelAl enviar tus consultas o comentarios estás accediendo a recibir nuestro newsletter de forma mensual.



AGREGAR UN COMENTARIO